Wie ist die Mischgleichmäßigkeit der Vormischung zu bewerten?
Am 18. Februar 2022 hat das Center for Drug Evaluation (CDE) die „Technischen Richtlinien für die Forschung zur Homogenität oraler fester Dosierungsformen und zur Homogenität der zentralen Kontrolleinheit (Studie)“ herausgegeben, im Folgenden als „Richtlinien“ bezeichnet. Die Leitlinien konzentrieren sich auf den abschließenden Mischprozess, der ebenfalls auf dem Gesamtkonzept „Quality by Design“ basiert. Dies liegt daran, dass die Homogenität der Endmischung vor den Press- oder Abfüllvorgängen die Grundlage für die Gewährleistung der Einheitlichkeit des Inhalts des Endprodukts ist und auch die optimale Phase für die Probenahme und Durchführung von Homogenitätsstudien darstellt. Grundsätzlich sollte die Homogenitätsstudie dieser Phase nicht übersprungen werden und die Prüfung der Inhaltshomogenität des Endprodukts sollte nicht direkt durchgeführt werden. Natürlich kann jeder Mischvorgang während des Produktionsprozesses auf Homogenität bewertet werden, die Anforderungen und Standards für Homogenität in anderen Prozessen werden in diesen Richtlinien jedoch nicht explizit spezifiziert. Der Autor teilt einige Erkenntnisse und Diskussionen, die auf praktischen Erfahrungen basieren, die in der Arbeit gemacht wurden.
Zu den gängigen Produktionsverfahren für orale feste Darreichungsformen gehören die Nassgranulierung mit hoher Scherung, die einstufige Wirbelschichtgranulierung, die Trockengranulierung und die direkte Komprimierung/Abfüllung von Pulver. Die Mischverfahren bei der Herstellung oraler fester Darreichungsformen umfassen typischerweise mindestens zwei Mischschritte: Vormischen und Endmischen, wobei einige Produkte möglicherweise mehr als zwei Mischschritte erfordern. Während der endgültige Mischprozess im Allgemeinen über verschiedene Produktionsmethoden hinweg konsistent ist, variieren die Risikoniveaus während der Vormischphase aufgrund unterschiedlicher Produktionsprinzipien, was differenzierte Forschungsansätze zur Gleichmäßigkeit der Vormischung erforderlich macht. Gemäß der Ausgabe 2023 der GMP-Richtlinien – Abschnitt „Oral Solid Dosage Forms“ gibt es keine zwingende Anforderung, die Mischgleichmäßigkeit während des Vormischens (falls zutreffend) zu bewerten. Die richtige Bestimmung des Umfangs der Mischungsgleichmäßigkeitsforschung ist für die Produktentwicklungskosten und die Qualitätskontrolle von entscheidender Bedeutung.
I. Nassgranulation mit hoher Scherung
Bei Verwendung des Nassgranulierungsverfahrens mit hoher Scherung sollte der Vormischschritt idealerweise im Nassgranulator durchgeführt werden. Alternativ können die Materialien zunächst in einem Mischer gemischt werden, bevor sie in den Granulator überführt werden. Sofern das Produkt keine besonderen Anforderungen stellt, wird das Vormischen im Granulator empfohlen, da es den Materialtransfer und den Mischerverbrauch reduziert und so einen effizienteren Arbeitsablauf gewährleistet. Für die Nassgranulierung mit hoher Scherung ist das Vormischen in der Regel unerlässlich, da es das Risiko ungleichmäßiger Nassgranulate in nachfolgenden Verarbeitungsstufen minimiert.
Probenahmegrundsätze auf Basis von Leitprinzipien: Probenahmestellen sollen gleichmäßig verteilt und repräsentativ sein. Unter Berücksichtigung der strukturellen Eigenschaften der Mischausrüstung sollten die Totzonen der Mischausrüstung identifiziert werden, um sicherzustellen, dass alle Materialien abgedeckt werden und gleichzeitig die Worst-Case-Standorte dargestellt werden. Die Vormisch-Probenahmestellen im Nassgranulator sind in der folgenden Abbildung dargestellt.
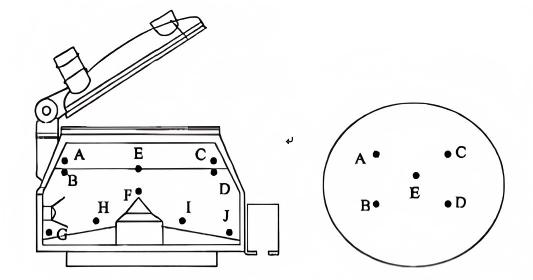
Die Homogenität des Vormischens wird im Allgemeinen von vier Faktoren beeinflusst: Materialbeladungsvolumen, Rührgeschwindigkeit, Schergeschwindigkeit und Mischzeit, mit möglichen Wechselwirkungen zwischen ihnen. Die Durchführung einer Versuchsplanung (Design of Experiments, DOE) würde eine übermäßige Anzahl von Versuchen erfordern. Das Ladevolumen kann auf der Grundlage der endgültigen Registrierungschargengröße berechnet werden, um die Konsistenz zwischen Laborchargen und zukünftigen Registrierungschargen sicherzustellen. Rührgeschwindigkeit und Schergeschwindigkeit können durch Berücksichtigung des Mischzustands der Materialien und des Verhältnisses des Rührpaddelradius zwischen Geräten im Pilotmaßstab und mittleren Maßstab bestimmt werden. Dieser Ansatz reduziert multifaktorielle Variablen für die Analyse auf einen einzigen Parameter – die Mischzeit.
Die Anfangsphase umfasst Laborstudien, um zu bewerten, wie sich unterschiedliche Vormischdauern auf die Produktgleichmäßigkeit auswirken, und so die Ermittlung optimaler Parameter zu ermöglichen. Diese Parameter werden dann während der Produktion im Pilotmaßstab validiert. In Pilotbetrieben werden in verschiedenen Vormischintervallen Proben gesammelt, um die Konsistenz zu beurteilen und die Kompatibilität zwischen Labor- und Pilotmischzeiten sicherzustellen. Für die Prozessvalidierung ist nur ein Zeitpunkt erforderlich, da Vormischparameter typischerweise als feste Werte und nicht als Bereiche festgelegt werden. Insbesondere wird in dieser Phase häufig auf die Validierung der Vormischungsgleichmäßigkeit verzichtet (insbesondere bei risikoarmen Produkten mit angegebenen Mengen > 25 mg oder einem Wirkstoffgehalt > 25 %), da die Mischdauer in der Pilotproduktion vorab festgelegt wird und anschließend ein Test der Gesamtmischungsgleichmäßigkeit durchgeführt wird.
Basierend auf unserer Erfahrung in der Forschung und Entwicklung von Laborgeräten haben wir vorläufige Richtlinien für die optimale Mischzeit erstellt. Bei der Gleichmäßigkeitsprobenahme vor dem Mischen von Pilotchargen müssen wir nicht mehr gemäß den Standardprotokollen drei Proben pro Punkt sammeln. Diese Anpassung ist darauf zurückzuführen, dass sich die Bewertung der Pilotcharge auf die Beurteilung konzentriert, wie sich unterschiedliche Mischdauern auf die Gleichmäßigkeit auswirken. Selbst wenn die RSD (Relative Standardabweichung) zu niedrigeren Zeitpunkten signifikant erscheint, besteht keine Notwendigkeit, die verbleibenden zwei Proben anhand der Messergebnisse zu validieren. Stattdessen sollten wir den optimalen Zeitpunkt auswählen, der die höchste Gleichmäßigkeit aufweist.
Wenn bei Teilchargen-Granulationsprodukten die Gleichmäßigkeit der Vormischung der Teilchargen in Pilotchargen mit guter Reproduzierbarkeit zwischen den Teilchargen untersucht wurde, deutet dies auf stabile Vormischprozesse hin. Selbst bei Produkten mit einem Gehalt an pharmazeutischen Wirkstoffen (API) von weniger als 25 % gelten die Risiken vor dem Mischen als gering, und die Validierung der Gleichmäßigkeit vor dem Mischen kann bei Prozessvalidierungschargen weggelassen werden. Das Personal an vorderster Front sollte sich darüber im Klaren sein, dass die Validierungsphase außergewöhnlich große Probenmengen und Testmengen unter engen Zeitvorgaben erfordert. Durch die Risikobewertung können wir Ressourcen risikoreichen Prozessen zuweisen, um die Produktqualität besser zu kontrollieren.
II. Einstufige Granulierung im Wirbelbett
Bei der einstufigen Wirbelschichtgranulierung ist ein Vormischen im Allgemeinen nicht erforderlich. Das zu granulierende Material wird in das Wirbelbett eingespeist und durchläuft dort eine Vorwärmphase (Temperatur je nach Produkteigenschaften angepasst), um eine anfängliche Durchmischung zu erreichen. Nach der Vorwärmphase ist keine Gleichmäßigkeitsprüfung erforderlich, sodass eine direkte Granulierung in einem Schritt möglich ist. Dieser Prozess nutzt das Funktionsprinzip des Wirbelbetts, bei dem das Material in einem kontinuierlichen Siedezustand bleibt und während der Vorheiz- und Granulierungsphase eine kräftige Durchmischung stattfindet.
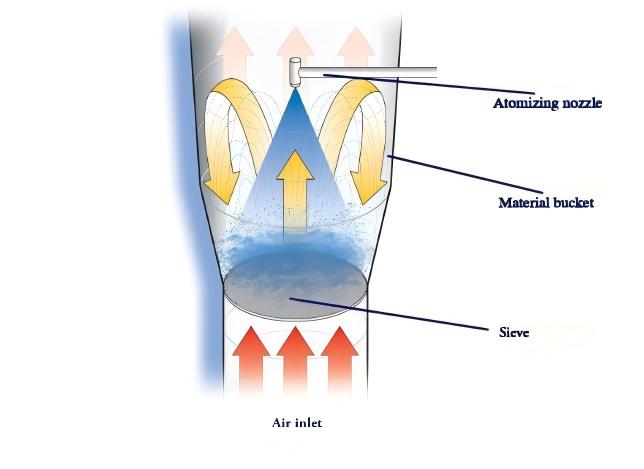
Während der Vorwärmphase kann das Fehlen einer Bindemittelzugabe zu einer Schichtung zwischen Materialien unterschiedlicher Dichte führen, wodurch eine Beurteilung der Gleichmäßigkeit nach dem Vorwärmen unpraktisch wird. In der anschließenden Granulierungsphase werden durch Zerstäuben und Einbringen des Bindemittels Materialien unterschiedlicher Dichte miteinander verbunden, wodurch nach und nach homogene Partikel entstehen. Nach der Granulierung und Trocknung sind Vorgänge wie das Rückblasen von Beutelfiltern erforderlich, um die Produktausbeute zu verbessern. Folglich verbleiben nach dem Abschalten der Maschine zwangsläufig Reste von feinem Pulver oder kleinen Partikeln in der oberen Materialschicht. Daher entspricht die durch einstufige Wirbelschichtgranulierung erzielte Gehaltsgleichmäßigkeit möglicherweise nicht den in den Richtlinien festgelegten Anforderungen.
Partikel, die durch einstufige Wirbelschichtgranulierung hergestellt werden, können einer Trockengranulierung unterzogen werden oder direkt dem Masterbatch-Prozess zugeführt werden, der einen gleichmäßigen Inhalt vor dem Komprimieren/Abfüllen der Tablette gewährleistet. Daher kann bei einstufigen Wirbelschichtgranulationsprozessen – sei es für Pilottests, die Produktion im Pilotmaßstab oder für die Prozessvalidierung – auf die Kontrolle und Validierung der Inhaltsgleichmäßigkeit verzichtet werden, wobei der Schwerpunkt stärker auf der Ausbeutestabilität liegt. Wenn weiterhin Bedenken hinsichtlich der Einheitlichkeit des Inhalts bestehen, ist es ratsam, Daten für eine retrospektive Analyse zu sammeln, anstatt strenge Akzeptanzkriterien festzulegen.
III. Trockengranulation
Bei Trockengranulierungsprozessen ist das Vormischen für die Erzielung einer gleichmäßigen Partikelgröße von entscheidender Bedeutung und erfordert gezielte Forschung. Im Gegensatz zur einstufigen Wirbelschichtgranulierung weist die Trockengranulierung eine schwächere Mischeffizienz auf. Mit der Schneckenförderstufe wird nur eine örtliche Vermischung erreicht, und der Mischzustand der in den Trichter zugeführten Materialien bestimmt letztendlich die Gleichmäßigkeit des trockenen Granulats.
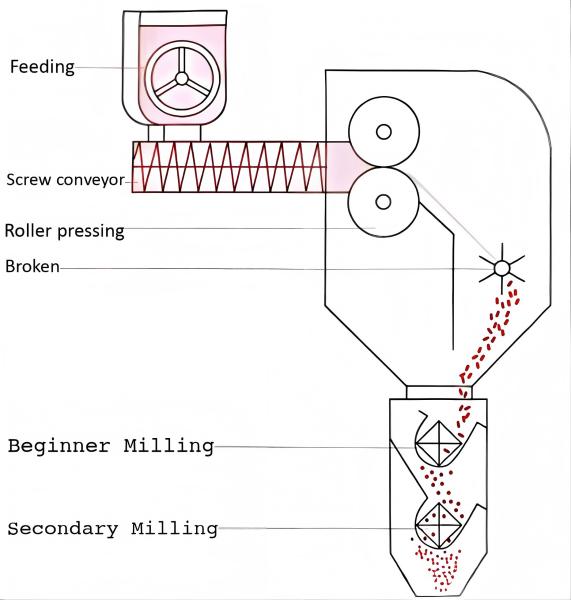
Für den Fall der Trockengranulierung nach dem Mischen des Pulvers stimmen die Vormischstudie und die Gesamtmischstudie im Wesentlichen überein. Da derselbe Mischer sowohl zum Vormischen als auch zum Gesamtmischen verwendet werden kann, treten bei der Trockengranulierung nach dem Pulvermischen im Allgemeinen keine Probleme mit Teilchargen auf. Die Probenahmepositionen von Mischern mit unterschiedlichen Prinzipien sind in der folgenden Abbildung dargestellt.
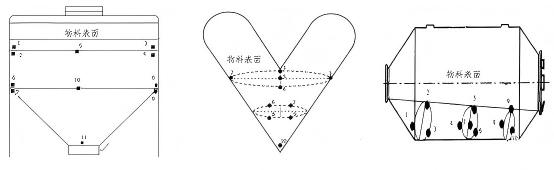
Die Trockengranulierung wird hauptsächlich bei der einstufigen Wirbelschichtgranulierung angewendet, wenn bestimmte Produkttypen eine geringe Dichte aufweisen (z. B. feste Dispersionen, die im Wirbelbett hergestellt werden) und für eine erfolgreiche Abfüllung oder Tablettenkomprimierung eine Dichteerhöhung durch Trockengranulierung erforderlich ist. In Wirbelschichtsystemen kann es zu einer Teilchargenverarbeitung kommen. Da die Trockengranulierung typischerweise externe Zusatzstoffe erfordert, können vor der Verarbeitung mehrere Teilchargen von Wirbelschichtmaterialien mit diesen Zusatzstoffen kombiniert werden. Die Beurteilung der Gleichmäßigkeit der Vormischung der kombinierten Materialien folgt der gleichen Methodik wie das vorherige Pulvermischverfahren.
Ähnlich wie beim Hochscher-Nassgranulationsverfahren können anhand der Registrierungscharge die gleiche Vormischungsbeladungsmenge und die gleiche feste Mischgeschwindigkeit ermittelt werden. Von Pilotversuchen im Labor bis hin zu Pilotversuchen in der Werkstatt kann nur der Einfluss der Mischzeit untersucht werden. Basierend auf Pilotversuchen im Labor wird die geeignete Vormischzeit während der Pilotcharge bestätigt. Bei Produkten mit geringem Risiko wird während der Prozessvalidierungsphase nur eine einmalige Überprüfung der Gleichmäßigkeit der Vormischung durchgeführt, und die Überprüfung der Gleichmäßigkeit der Vormischung kann weggelassen werden.
IV. Direktes Pressen/Abfüllen von Pulvern
Der Pulver-Direktkompressions-/Abfüllprozess erfordert hohe Materialeigenschaften für die Formulierungsqualität. Typischerweise gibt es zwei Mischstufen: Vormischen und Endmischen, wobei der Endstufe mehrere Mischschritte vorausgehen. In den meisten Fällen wird beim letzten Mischschritt nur eine kleine Menge Gleitmittel oder Fließhilfsmittel hinzugefügt. Daher ist es wichtig, die Gleichmäßigkeit der Mischung vor dem endgültigen Mischen durch Vormischungs- und Mischuntersuchungen zu beurteilen. Siehe das schematische Diagramm der Probenahme im Abschnitt zur Trockengranulierung.
Die Untersuchung der Homogenität im Vormisch-/Mischprozess zielt in erster Linie darauf ab, geeignete Mischzeitparameter zu identifizieren. Angesichts der begrenzten Anzahl direkter Pulverpress-/Abfüllprozesse kann die Prozessvalidierungsproduktion gleichzeitig sowohl das Vormischen/Mischen als auch das Endmischen validieren, um die Risikokontrollmöglichkeiten für den Herstellungsprozess zu verbessern.
Der Direktkompressions-/Abfüllprozess des Pulvers kann mehrere Mischschritte umfassen, und manuelles Mischen in jedem dieser Schritte sollte nach Möglichkeit vermieden werden. Bei Hochrisikoprodukten kann die Reproduzierbarkeit der kommerziellen Produktion aufgrund unterschiedlicher Bedienerkenntnisse möglicherweise nicht gewährleistet werden.
V. Vorsichtsmaßnahmen für gemischte Prozesse
5.1 Akzeptanzkriterien
Bei herkömmlichen Arzneimitteln muss die Gesamtgleichmäßigkeit der Mischung im Allgemeinen innerhalb von ±10 % (absolut) des Mittelwerts liegen, mit einem Variationskoeffizienten (RSD) ≤5 %. Bei Arzneimitteln mit engem therapeutischen Index (NTI) oder hochaktiven Arzneimitteln, bei denen die Genauigkeit der Einzeldosen die Wirksamkeit und Sicherheit des Arzneimittels erheblich beeinflusst, wird empfohlen, dass Formulierungsantragsteller/Arzneimittelhersteller auf der Grundlage wissenschaftlicher Erkenntnisse und Risikobewertung des Produkts strengere Probenahmepläne erstellen, Studien zur Mischungsgleichmäßigkeit durchführen und strengere Akzeptanzkriterien entwickeln. Wenn der RSD beispielsweise auf 2 % oder sogar weniger festgelegt wird und ein Variationskoeffizient (CV) von <10 % für NTI-Arzneimittel angenommen wird, würde eine Inhaltseinheitlichkeit von 4,5 % ein erhebliches Risiko einer Nichtäquivalenz der Bioäquivalenz (BE) darstellen. Weitere Informationen finden Sie im Abschnitt zur Äquivalenzanalyse in der grundlegenden Logik des Arzneimittels BE mit engem therapeutischen Fenster. Unabhängig vom Zubereitungsprozess ist es ideal, den gleichen Standard für die Gleichmäßigkeit des Vormischens wie für die Gleichmäßigkeit des gesamten Mischens zu erreichen. Wenn die Gleichmäßigkeit der Vormischung die relevanten Normen nicht erfüllen kann, besteht kein Grund zur Sorge, da der akzeptable Bereich für die Gleichmäßigkeit der Vormischung breiter sein kann als die in den Richtlinien festgelegten Anforderungen, vorausgesetzt, dass die Gleichmäßigkeit der Gesamtmischung den Anforderungen der Richtlinie entspricht.
5,2 Mischzeit
In der Praxis umfasst das vollständige Mischen typischerweise nur die Zugabe von Magnesiumstearat als Schmiermittel mit einem Gewichtsprozentsatz von etwa 1 %. Einige Praktiker aus der Industrie haben beobachtet, dass die Gesamtmischdauer auf 1 oder 2 Minuten festgelegt wird, da die Homogenität der vorherigen Mischstufe bereits vor dem vollständigen Mischen überprüft wurde. Selbst wenn Magnesiumstearat während des Gesamtmischens ungleichmäßig verteilt ist, können solche Inkonsistenzen durch den Homogenitätstest des Gesamtmischens nicht erkannt werden. Die Gesamtmischdauer von 1 oder 2 Minuten kann lediglich als psychologische Beruhigung dienen. Inhomogenes Magnesiumstearat kann zu unterschiedlichen Auflösungen von Charge zu Charge führen und auch zu Haftungsproblemen führen, die möglicherweise eine erhöhte Dosierung von Magnesiumstearat erforderlich machen.
Wie soll diese gestaltet sein? Für Formulierungen ohne übermäßige Schmierprobleme (bei denen die Tablettenhärte unter den Erwartungen liegt oder die Auflösung verringert ist) wird empfohlen, alle externen Materialien, einschließlich Magnesiumstearat, zum gleichzeitigen Mischen in den Masterbatch einzuarbeiten. Durch diesen Ansatz entfällt nicht nur ein Verarbeitungsschritt, sondern auch die Notwendigkeit zweier separater Homogenitätsbewertungen. Für Formulierungen, die möglicherweise zu übermäßiger Schmierung neigen, kann dennoch eine einstufige Mischmethode angewendet werden, um die kürzeste Mischzeit für Gleichmäßigkeit zu erreichen. Anschließend kann Magnesiumstearat während der abschließenden Masterbatch-Mischung entsprechend diesem optimalen Zeitpunkt zugegeben werden. Wenn die kürzeste Mischzeit das Problem der übermäßigen Schmierung nicht löst (vorausgesetzt, es handelt sich tatsächlich um eine übermäßige Schmierung und nicht um eine durch andere Faktoren verursachte Fehleinschätzung), sollten alternative Schmierstoffe in Betracht gezogen werden.
5.3 Anzahl der Proben
Gemäß den Richtlinien sollten für Masterbatch an jeder Probenahmestelle mindestens drei Proben entnommen werden. Bei einigen Produkten ist möglicherweise eine zusätzliche Prüfung der Masterbatch-Gleichmäßigkeit als Teil der Qualitätsstandards für Zwischenprodukte erforderlich, was eine Kontrolle der Inhaltsgleichmäßigkeit während der zukünftigen kommerziellen Produktion erforderlich macht. Für Vormischungen, die typischerweise nur während der F&E-Phase durchgeführt werden und Forschungscharakter haben, sind 1 bis 2 Proben pro Punkt (zur Sicherung) ausreichend.
Das Probenahmevolumen für eine einzelne Probe sollte typischerweise zwischen dem 1- und 10-fachen der Einheitsdosis liegen. Für die Homogenitätsprüfung muss die gesamte Probe verwendet werden, um eine Zweitprobenahme zu vermeiden. Wenn das Probenahmevolumen das Dreifache der Einheitsdosis übersteigt, muss eine wissenschaftliche Begründung oder ein Nachweis vorgelegt werden. Dies liegt daran, dass ein Probenvolumen, das mehr als das Dreifache der Einheitsdosis beträgt, die Tatsache einer ungleichmäßigen Vermischung aufgrund einer übermäßigen Probenmenge verschleiern kann.
VI. Abschluss
In den Leitlinien heißt es, dass die Forschung an Sorten durchgeführt werden sollte, die bei Misch- oder Press-/Abfüllprozessen als mittel- bis hochrisikobehaftet eingestuft werden, und zwar auf der Grundlage des Prinzips der Risikobewertung in Kombination mit den Merkmalen des Produkts und des Produktionsprozesses. Beispielsweise verlangt das Chinesische Arzneibuch die Untersuchung der Mischgleichmäßigkeit für chemische orale feste Darreichungsformen (gekennzeichnete Menge <25 mg oder Wirkstoffgehalt <25 %), die eine Prüfung der Inhaltsgleichmäßigkeit erfordern, da ihr Mischrisiko relativ hoch ist. Daher können bei Sorten mit geringem Risiko einige Prozessstudien vor dem Mischen reduziert werden.
Ganz gleich, ob es sich um Vormischungs- oder Endmischungsprozesse handelt, alle müssen einer strengen Bewertung und Prüfung nach strengsten Standards unterzogen werden. Daran besteht kein Zweifel – schließlich beschweren sich CDE-Rezensenten nicht über übermäßige Recherche. Produktionsleiter werden sich jedoch auf Effizienz und Kosten konzentrieren, insbesondere bei zwischenzeitlichen Prozessinspektionen für die zukünftige kommerzielle Produktion. Wenn eine QC-Genehmigung für Zwischenprodukte vor der Weiterverarbeitung obligatorisch ist, verringert dies nicht nur die Produktionseffizienz, sondern weicht auch vom Prinzip der Qualität durch Design ab. Als Arzneimittelentwickler müssen wir sowohl die Forschungs- und Entwicklungsphase als auch die kommerzielle Produktionsphase berücksichtigen. Basierend auf Produkteigenschaften und Risikobewertungen sollten wir geeignete Qualitätskontrollstrategien festlegen, einschließlich positionsspezifischer Kontrollen und Ersatzindikatoren.


















