Comment évaluer l’uniformité du mélange du prémélange ?
Le 18 février 2022, le Centre d'évaluation des médicaments (CDE) a publié les « Lignes directrices techniques pour la recherche sur l'homogénéité des formes posologiques solides orales et l'homogénéité de l'unité de contrôle centrale (essai) », ci-après dénommées les « Lignes directrices ». Les lignes directrices se concentrent sur le processus de mélange final, qui repose également sur le concept global de qualité dès la conception. En effet, l'homogénéité du mélange final avant les opérations de compression ou de remplissage est la base pour garantir l'uniformité du contenu du produit final, et c'est également l'étape optimale pour l'échantillonnage et la réalisation d'études d'homogénéité. En principe, l'étude d'homogénéité de cette étape ne doit pas être ignorée et les tests d'homogénéité du contenu du produit final ne doivent pas être effectués directement. Bien entendu, l'homogénéité de toute opération de mélange au cours du processus de production peut être évaluée, mais les exigences et les normes d'homogénéité dans d'autres processus ne sont pas explicitement spécifiées dans ces directives. L'auteur partage quelques idées et discussions basées sur des expériences pratiques rencontrées dans le cadre de son travail.
Les processus de production courants pour les formes posologiques orales solides comprennent la granulation humide à cisaillement élevé, la granulation en une étape sur lit fluidisé, la granulation sèche et la compression/remplissage direct de poudre. Les procédures de mélange dans la production de formes posologiques solides orales impliquent généralement au moins deux étapes de mélange : le prémélange et le mélange final, certains produits nécessitant potentiellement plus de deux étapes de mélange. Bien que le processus de mélange final soit généralement cohérent entre les différentes méthodes de production, les niveaux de risque au cours de l'étape de prémélange varient en raison de principes de production différents, ce qui nécessite des approches de recherche différenciées pour l'uniformité du prémélange. Selon l'édition 2023 de la section Lignes directrices BPF – Formes posologiques solides orales, il n'y a aucune exigence obligatoire pour évaluer l'uniformité du mélange pendant le prémélange (le cas échéant). Déterminer correctement l'étendue de la recherche sur l'uniformité du mélange est essentiel pour les coûts de développement de produits et le contrôle qualité.
I. Granulation humide à cisaillement élevé
Lors de l’utilisation du procédé de granulation humide à cisaillement élevé, l’étape de prémélange doit idéalement être effectuée dans le granulateur humide. Alternativement, les matériaux peuvent d'abord être mélangés dans un mélangeur avant d'être transférés au granulateur. Sauf si le produit a des exigences spécifiques, le prémélange dans le granulateur est recommandé car il réduit le transfert de matériaux et l'utilisation du mélangeur, garantissant ainsi un flux de travail plus efficace. Pour la granulation humide à cisaillement élevé, le prémélange est généralement essentiel, car il minimise le risque de granulés humides irréguliers lors des étapes de traitement ultérieures.
Principes d'échantillonnage basés sur des principes directeurs : les points d'échantillonnage doivent être uniformément répartis et représentatifs. Compte tenu des caractéristiques structurelles de l'équipement de mélange, les zones mortes de l'équipement de mélange doivent être identifiées pour garantir la couverture de tous les matériaux tout en représentant les emplacements les plus défavorables. Les points d'échantillonnage de pré-mélange à l'intérieur du granulateur humide sont illustrés dans la figure ci-dessous.
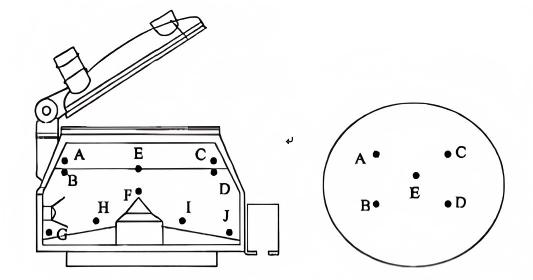
L'homogénéité du prémélange est généralement influencée par quatre facteurs : le volume de chargement du matériau, la vitesse d'agitation, le taux de cisaillement et le temps de mélange, avec des interactions potentielles entre eux. La réalisation d’un plan d’expériences (DOE) nécessiterait un nombre excessif d’essais. Le volume de chargement peut être calculé en fonction de la taille finale du lot d’enregistrement afin de garantir la cohérence entre les lots de laboratoire et les futurs lots d’enregistrement. La vitesse d'agitation et le taux de cisaillement peuvent être déterminés en tenant compte de l'état de mélange des matériaux et du rapport entre le rayon de la palette d'agitation entre les équipements à échelle pilote et intermédiaire. Cette approche réduit les variables multifactorielles à un seul paramètre (le temps de mélange) pour l'analyse.
La phase initiale implique des études en laboratoire pour évaluer comment différentes durées de prémélange affectent l'uniformité du produit, permettant ainsi l'identification des paramètres optimaux. Ces paramètres sont ensuite validés lors d’une production à l’échelle pilote. Dans les opérations pilotes, des échantillons sont collectés à différents intervalles de pré-mélange pour évaluer la cohérence, garantissant ainsi la compatibilité entre les temps de mélange en laboratoire et à l'échelle pilote. Pour la validation du processus, un seul instant est requis, car les paramètres de prémélange sont généralement définis sous forme de valeurs fixes plutôt que de plages. Notamment, la validation de l'uniformité du prémélange est souvent omise à cette étape (en particulier pour les produits à faible risque avec des quantités étiquetées > 25 mg ou une teneur en ingrédient actif > 25 %), puisque la durée du mélange est prédéterminée dans la production pilote et que des tests d'uniformité totale du mélange seront ensuite effectués.
Sur la base de notre expérience en R&D en matière d’équipements de laboratoire, nous avons établi des lignes directrices préliminaires pour un temps de mélange optimal. Lors de l’échantillonnage d’uniformité du pré-mélange du lot pilote, nous n’avons plus besoin de collecter trois échantillons par point selon les protocoles standard. Cet ajustement est dû au fait que l'évaluation du lot pilote se concentre sur l'évaluation de la manière dont les différentes durées de mélange affectent l'uniformité. Même lorsque l'écart type relatif (RSD) à des moments inférieurs semble significatif, il n'est pas nécessaire de valider les deux échantillons restants sur la base des résultats de mesure. Au lieu de cela, nous devrions sélectionner le moment optimal qui démontre la plus grande uniformité.
Pour les produits de granulation en sous-lots, si l'uniformité du pré-mélange des sous-lots a été étudiée dans des lots pilotes avec une bonne reproductibilité entre les sous-lots, cela indique des processus de pré-mélange stables. Même pour les produits dont la teneur en ingrédients pharmaceutiques actifs (API) est inférieure à 25 %, les risques de pré-mélange sont considérés comme faibles et la validation de l'uniformité du pré-mélange peut être omise dans les lots de validation du processus. Le personnel de première ligne doit être conscient que la phase de validation implique des volumes d'échantillons exceptionnellement importants et des quantités de tests dans des délais serrés. Grâce à l'évaluation des risques, nous pouvons allouer des ressources aux processus à haut risque pour mieux contrôler la qualité des produits.
II. Granulation en une étape en lit fluidisé
Dans la granulation en une étape en lit fluidisé, le pré-mélange est généralement inutile. Le matériau à granuler est introduit dans le lit fluidisé, où il subit une phase de préchauffage (température ajustée en fonction des caractéristiques du produit) pour obtenir un premier mélange. Aucun test d'uniformité n'est requis après l'étape de préchauffage, permettant une granulation directe en une seule étape. Ce processus exploite le principe de fonctionnement du lit fluidisé, dans lequel le matériau reste dans un état d'ébullition continu, avec un mélange vigoureux se produisant tout au long des phases de préchauffage et de granulation.
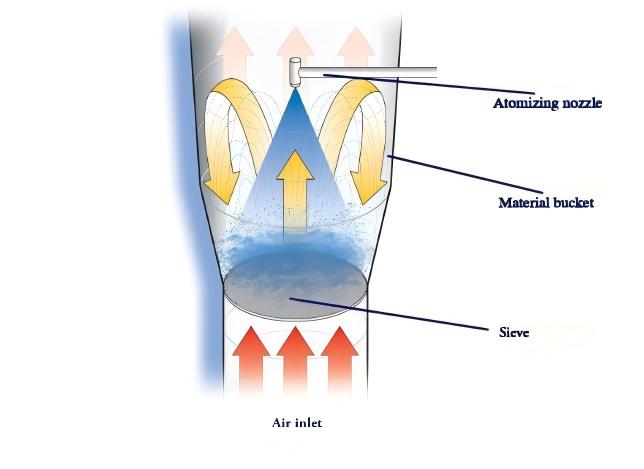
Pendant l'étape de préchauffage, l'absence d'ajout de liant peut provoquer une stratification entre des matériaux de densités différentes, rendant impossible l'évaluation de l'uniformité après préchauffage. Dans la phase de granulation suivante, au fur et à mesure que le liant est atomisé et introduit, des matériaux de densités variables sont liés entre eux, formant progressivement des particules homogènes. Après la granulation et le séchage, des opérations telles que le rétro-soufflage du filtre à manches sont nécessaires pour améliorer le rendement du produit. Par conséquent, la poudre fine résiduelle ou les petites particules restent inévitablement dans la couche supérieure du matériau après l'arrêt de la machine. Par conséquent, l’uniformité du contenu obtenue grâce à la granulation en lit fluidisé en une seule étape peut ne pas répondre aux exigences spécifiées dans les lignes directrices.
Les particules produites par granulation en une étape sur lit fluidisé peuvent subir une granulation sèche ou passer directement au processus de mélange maître, qui garantit un contenu uniforme avant la compression/remplissage du comprimé. Par conséquent, dans les processus de granulation en une étape en lit fluidisé, que ce soit pour des tests pilotes, une production à échelle pilote ou une validation de processus, le contrôle et la validation de l'uniformité du contenu peuvent être omis, l'accent étant davantage mis sur la stabilité du rendement. Si les problèmes d’uniformité du contenu persistent, il est conseillé de collecter des données pour une analyse rétrospective plutôt que d’établir des critères d’acceptation stricts.
III. Granulation sèche
Dans les processus de granulation sèche, le prémélange est essentiel pour obtenir une taille de particule uniforme, ce qui nécessite des recherches ciblées. Contrairement à la granulation en une étape sur lit fluidisé, la granulation sèche démontre une efficacité de mélange plus faible. L'étape du convoyeur à vis ne réalise qu'un mélange localisé, et les conditions de mélange des matériaux introduits dans la trémie déterminent en fin de compte l'uniformité des granulés secs.
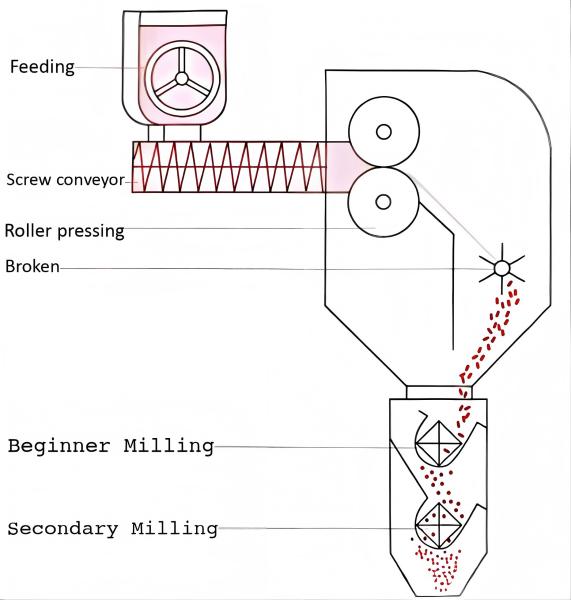
Pour le cas de granulation sèche après mélange de poudres, l’étude de pré-mélange et l’étude de mélange total sont essentiellement cohérentes. Étant donné que le même mélangeur peut être utilisé à la fois pour le pré-mélange et le mélange total, les problèmes de sous-lots ne se produisent généralement pas lors de la granulation sèche après le mélange de la poudre. Les positions d'échantillonnage des mélangeurs avec différents principes sont indiquées dans la figure ci-dessous.
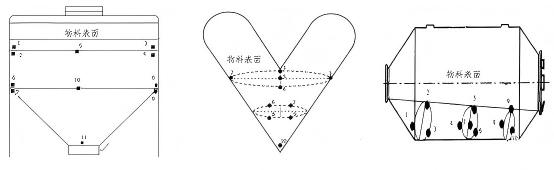
La granulation sèche est principalement appliquée à la granulation en lit fluidisé en une seule étape lorsque certains types de produits présentent une faible densité (par exemple, des dispersions solides préparées via un lit fluidisé), nécessitant une amélioration de la densité par granulation sèche pour un remplissage ou une compression réussie des comprimés. Un traitement en sous-lots dans des systèmes à lit fluidisé peut avoir lieu. Étant donné que la granulation sèche nécessite généralement des additifs externes, plusieurs sous-lots de matériaux à lit fluidisé peuvent être combinés avec ces additifs avant le traitement. L'évaluation de l'uniformité du pré-mélange pour les matériaux combinés suit la même méthodologie que la procédure précédente de mélange de poudres.
Semblable au processus de granulation humide à cisaillement élevé, la même quantité de chargement de prémélange et la même vitesse de mélange fixe peuvent être déterminées en fonction du lot d'enregistrement. Des essais pilotes en laboratoire aux essais pilotes en atelier, seul l’impact du temps de mélange peut être étudié. Sur la base de recherches pilotes en laboratoire, le temps de prémélange approprié est confirmé lors du lot pilote. Pour les produits à faible risque, une seule vérification ponctuelle de l’uniformité du prémélange est effectuée pendant la phase de validation du processus, et la vérification de l’uniformité du prémélange peut être omise.
IV. Pressage/Remplissage Direct de Poudres
Le processus de compression/remplissage direct de poudre nécessite des propriétés matérielles élevées pour la qualité de la formulation. Généralement, il y a deux étapes de mélange : le prémélange et le mélange final, avec plusieurs étapes de mélange précédant l'étape finale. Dans la plupart des cas, seule une petite quantité de lubrifiant ou d’aide à l’écoulement est ajoutée lors de l’étape finale de mélange. Par conséquent, il est essentiel d’évaluer l’uniformité du mélange au moyen d’enquêtes de prémélange et de mélange avant le mélange final. Voir le diagramme schématique d’échantillonnage sous la section granulation sèche.
L'étude de l'homogénéité dans le processus de prémélange/mélange vise principalement à identifier les paramètres de temps de mélange appropriés. Compte tenu du nombre limité de processus de pressage/remplissage direct de poudre, la production de validation des processus peut valider simultanément à la fois le prémélange/mélange et le mélange final afin d'améliorer les capacités de contrôle des risques pour le processus de fabrication.
Le processus de compression/remplissage direct de la poudre peut impliquer plusieurs étapes de mélange, et le mélange manuel dans l'une de ces étapes doit être évité autant que possible. Pour les produits à haut risque, la reproductibilité de la production commerciale peut ne pas être garantie en raison des différences dans les compétences des opérateurs.
V. Précautions pour les procédés mixtes
5.1 Critères d'acceptation
Pour les médicaments conventionnels, l'uniformité totale du mélange doit généralement se situer à ± 10 % (en absolu) de la valeur moyenne, avec un coefficient de variation (RSD) ≤ 5 %. Pour les médicaments à index thérapeutique étroit (NTI) ou les médicaments hautement actifs, pour lesquels l'exactitude des doses unitaires a un impact significatif sur l'efficacité et la sécurité des médicaments, il est recommandé aux demandeurs de formulation/fabricants pharmaceutiques, sur la base de la compréhension scientifique et de l'évaluation des risques du produit, d'établir des plans d'échantillonnage plus stricts, de mener des études d'uniformité du mélange et d'élaborer des critères d'acceptation plus stricts. Par exemple, si le RSD est fixé à 2 % ou même moins, et en supposant un coefficient de variation (CV) < 10 % pour les médicaments NTI, une uniformité du contenu de 4,5 % poserait un risque important de non-équivalence de bioéquivalence (BE). Reportez-vous à la section sur l’analyse d’équivalence dans la logique fondamentale du médicament à fenêtre thérapeutique étroite BE. Quel que soit le processus de préparation, atteindre le même standard d’uniformité de pré-mélange que l’uniformité totale du mélange est un état idéal. Si l'uniformité du pré-mélange ne peut pas répondre aux normes pertinentes, il n'y a pas lieu de s'inquiéter, car la plage acceptable pour l'uniformité du pré-mélange peut être plus large que les exigences spécifiées dans les lignes directrices, à condition que l'uniformité totale du mélange soit conforme aux exigences des lignes directrices.
5.2 temps de mélange
En pratique, le mélange total implique généralement uniquement l'ajout de stéarate de magnésium comme lubrifiant, avec un pourcentage pondéral d'environ 1 %. Certains professionnels de l'industrie ont observé que les durées totales de mélange sont fixées à 1 ou 2 minutes, l'homogénéité de l'étape de mélange précédente ayant déjà été vérifiée avant le mélange total. Même si le stéarate de magnésium est inégalement réparti lors du mélange total, de telles incohérences ne peuvent pas être détectées par le test d'homogénéité du mélange total. La durée totale de mixage de 1 ou 2 minutes peut simplement servir de réconfort psychologique. Le stéarate de magnésium inhomogène peut entraîner des variations de dissolution d'un lot à l'autre et peut également entraîner des problèmes d'adhésion, nécessitant potentiellement une augmentation du dosage de stéarate de magnésium.
Comment cela devrait-il être conçu ? Pour les formulations sans problèmes de lubrification excessifs (où la dureté des comprimés est inférieure à celle attendue ou où la dissolution est réduite), il est recommandé d'incorporer tous les matériaux externes, y compris le stéarate de magnésium, dans le mélange maître pour un mélange simultané. Cette approche élimine non seulement une étape de traitement, mais évite également le besoin de deux évaluations d'homogénéité distinctes. Pour les formulations potentiellement sujettes à une lubrification excessive, une méthode de mélange en une étape peut toujours être utilisée pour obtenir le temps de mélange le plus court pour assurer l'uniformité. Le stéarate de magnésium peut ensuite être ajouté lors du mélange final du mélange maître en fonction de ce temps optimal. Si le temps de mélange le plus court ne parvient pas à résoudre le problème de lubrification excessive (en supposant que la lubrification est véritablement excessive plutôt qu'une erreur d'appréciation causée par d'autres facteurs), des lubrifiants alternatifs doivent être envisagés.
5.3 Nombre d'échantillons
Selon les directives, pour le mélange maître, au moins trois échantillons doivent être collectés à chaque point d'échantillonnage. Certains produits peuvent nécessiter des tests supplémentaires d'uniformité du mélange maître dans le cadre des normes de qualité des produits intermédiaires, ce qui nécessite un contrôle de l'uniformité du contenu lors de la production commerciale future. Pour les prémix, qui sont généralement réalisés uniquement pendant la phase de R&D et sont de nature recherche, 1 à 2 échantillons par point (en sauvegarde) suffisent.
Le volume d’échantillonnage pour un seul échantillon doit généralement être compris entre 1 et 10 fois la dose unitaire. L’échantillon entier doit être utilisé pour les tests d’homogénéité afin d’éviter un échantillonnage secondaire. Lorsque le volume de prélèvement dépasse 3 fois la dose unitaire, une justification ou une preuve scientifique doit être fournie. En effet, un volume d'échantillon supérieur à 3 fois la dose unitaire peut masquer le fait d'un mélange inégal dû à une quantité d'échantillon excessive.
VI. Conclusion
Les lignes directrices mentionnent que la recherche devrait être menée sur les variétés évaluées comme présentant un risque moyen à élevé dans les processus de mélange ou de compression/remplissage, sur la base du principe de l'évaluation des risques, combiné aux caractéristiques du produit et du processus de production. Par exemple, la Pharmacopée chinoise exige l'étude de l'uniformité du mélange pour les formes posologiques solides orales chimiques (quantité étiquetée <25 mg ou teneur en ingrédient actif <25 %) qui nécessitent des tests d'uniformité du contenu, car leur risque de mélange est relativement élevé. Par conséquent, pour les variétés à faible risque, certaines études sur le processus de pré-mélange peuvent être réduites.
Qu'il s'agisse de processus de pré-mélange ou de mélange final, tous doivent être soumis à une évaluation et à des tests rigoureux selon les normes les plus strictes. Cela ne fait aucun doute : après tout, les évaluateurs du CDE ne se plaindront pas d'une recherche excessive. Cependant, les directeurs de production se concentreront sur l’efficacité et les coûts, en particulier lors des inspections de processus intermédiaires en vue d’une future production commerciale. Si l’approbation du contrôle qualité est obligatoire pour les produits intermédiaires avant de continuer, cela réduit non seulement l’efficacité de la production, mais s’écarte également du principe de qualité dès la conception. En tant que développeurs de médicaments, nous devons prendre en compte à la fois les phases de R&D et de production commerciale. Sur la base des caractéristiques du produit et des évaluations des risques, nous devons établir des stratégies de contrôle qualité appropriées, y compris des contrôles spécifiques au poste et des indicateurs de substitution.


















