Come deve essere valutata l'uniformità di miscelazione del premiscelato?
Il 18 febbraio 2022, il Centro per la valutazione dei farmaci (CDE) ha pubblicato le 'Linee guida tecniche per la ricerca sull'omogeneità delle forme di dosaggio solide orali e sull'omogeneità dell'unità di controllo centrale (prova)', di seguito denominate le 'Linee guida'. Le Linee Guida si concentrano sul processo di miscelazione finale, che si basa anch'esso sul concetto generale di qualità fin dalla progettazione. Questo perché l'omogeneità della miscela finale prima delle operazioni di compressione o riempimento è la base per garantire l'uniformità del contenuto del prodotto finale ed è anche la fase ottimale per il campionamento e la conduzione di studi di omogeneità. In linea di principio, lo studio dell'omogeneità di questa fase non dovrebbe essere saltato e il test dell'uniformità del contenuto del prodotto finale non dovrebbe essere condotto direttamente. Naturalmente, qualsiasi operazione di miscelazione durante il processo di produzione può essere valutata per l'omogeneità, ma i requisiti e gli standard per l'omogeneità in altri processi non sono esplicitamente specificati in queste Linee Guida. L'autore condivide alcuni approfondimenti e discussioni basati sulle esperienze pratiche incontrate nel lavoro.
I processi di produzione comuni per le forme di dosaggio solide orali includono la granulazione umida ad alto taglio, la granulazione in un unico passaggio a letto fluidizzato, la granulazione a secco e la compressione/riempimento diretto della polvere. Le procedure di miscelazione nella produzione di forme di dosaggio solide orali comportano tipicamente almeno due fasi di miscelazione: premiscelazione e miscelazione finale, con alcuni prodotti che richiedono potenzialmente più di due fasi di miscelazione. Sebbene il processo di miscelazione finale sia generalmente coerente tra i diversi metodi di produzione, i livelli di rischio durante la fase di premiscelazione variano a causa dei diversi principi di produzione, richiedendo approcci di ricerca differenziati per l’uniformità della premiscelazione. Secondo l'edizione 2023 delle Linee guida GMP - Sezione Forme di dosaggio solide orali, non esiste alcun requisito obbligatorio per valutare l'uniformità di miscelazione durante la premiscelazione (se applicabile). Determinare correttamente l'entità della ricerca sull'uniformità della miscelazione è fondamentale per i costi di sviluppo del prodotto e il controllo di qualità.
I. Granulazione ad umido ad alto taglio
Quando si utilizza il processo di granulazione a umido ad alto taglio, la fase di premiscelazione dovrebbe idealmente essere eseguita all'interno del granulatore a umido. In alternativa, i materiali possono essere prima miscelati in un miscelatore prima di essere trasferiti al granulatore. A meno che il prodotto non abbia requisiti specifici, si consiglia la premiscelazione nel granulatore in quanto riduce il trasferimento di materiale e l'utilizzo del miscelatore, garantendo un flusso di lavoro più efficiente. Per la granulazione a umido ad alto taglio, la premiscelazione è generalmente essenziale, poiché riduce al minimo il rischio di granuli bagnati irregolari nelle successive fasi di lavorazione.
Principi di campionamento basati su principi guida: i punti di campionamento dovrebbero essere distribuiti uniformemente e rappresentativi. Considerando le caratteristiche strutturali dell'attrezzatura di miscelazione, le zone morte dell'attrezzatura di miscelazione dovrebbero essere identificate per garantire la copertura di tutti i materiali pur rappresentando le posizioni peggiori. I punti di campionamento della premiscelazione all'interno del granulatore ad umido sono mostrati nella figura seguente.
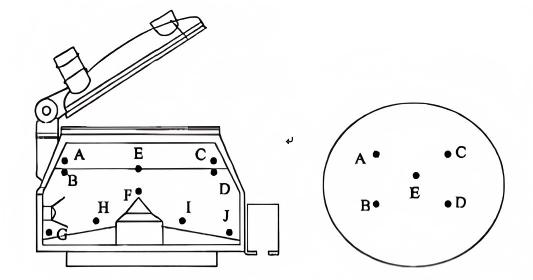
L'omogeneità della premiscelazione è generalmente influenzata da quattro fattori: volume di caricamento del materiale, velocità di agitazione, velocità di taglio e tempo di miscelazione, con potenziali interazioni tra loro. Condurre un disegno di esperimenti (DOE) richiederebbe un numero eccessivo di prove. Il volume di carico può essere calcolato in base alla dimensione finale del lotto di registrazione per garantire la coerenza tra i lotti di laboratorio e i futuri lotti di registrazione. La velocità di agitazione e la velocità di taglio possono essere determinate considerando lo stato di miscelazione dei materiali e il rapporto del raggio della pala di agitazione tra le apparecchiature su scala pilota e su scala intermedia. Questo approccio riduce le variabili multifattoriali a un singolo parametro, il tempo di miscelazione, per l'analisi.
La fase iniziale prevede studi di laboratorio per valutare come le diverse durate della premiscelazione influiscono sull'uniformità del prodotto, consentendo l'individuazione dei parametri ottimali. Questi parametri vengono poi convalidati durante la produzione su scala pilota. Nelle operazioni pilota, i campioni vengono raccolti a vari intervalli di premiscelazione per valutarne la consistenza, garantendo la compatibilità tra i tempi di miscelazione su scala pilota e di laboratorio. Per la convalida del processo, è richiesto un solo punto temporale, poiché i parametri di premiscelazione sono generalmente impostati come valori fissi anziché come intervalli. In particolare, la convalida dell'uniformità della premiscelazione viene spesso omessa in questa fase (in particolare per i prodotti a basso rischio con quantità indicate sull'etichetta > 25 mg o contenuto di principio attivo > 25%), poiché la durata della miscelazione è predeterminata nella produzione pilota e verranno successivamente condotti test di uniformità della miscelazione totale.
Sulla base della nostra esperienza in ricerca e sviluppo di apparecchiature di laboratorio, abbiamo stabilito linee guida preliminari per il tempo di miscelazione ottimale. Durante il campionamento dell'uniformità della premiscelazione del batch pilota, non è più necessario raccogliere tre campioni per punto come previsto dai protocolli standard. Questo aggiustamento è dovuto al fatto che la valutazione del lotto pilota si concentra sulla valutazione di come le diverse durate di miscelazione influiscono sull'uniformità. Anche quando la RSD (deviazione standard relativa) in momenti temporali inferiori appare significativa, non è necessario convalidare i due campioni rimanenti in base ai risultati della misurazione. Dovremmo invece selezionare il punto temporale ottimale che dimostra la massima uniformità.
Per i prodotti di granulazione in sottolotti, se l'uniformità di premiscelazione dei sottolotti è stata studiata in lotti pilota con buona riproducibilità tra sottolotti, ciò indica processi di premiscelazione stabili. Anche per i prodotti con un contenuto di principio attivo farmaceutico (API) inferiore al 25%, i rischi di premiscelazione sono considerati bassi e la convalida dell'uniformità della premiscelazione può essere omessa nei lotti di validazione del processo. Il personale in prima linea deve essere consapevole che la fase di convalida prevede volumi di campioni eccezionalmente grandi e quantità di test in tempi ristretti. Attraverso la valutazione del rischio, possiamo allocare risorse ai processi ad alto rischio per controllare meglio la qualità del prodotto.
II. Granulazione in un solo passaggio in letto fluido
Nella granulazione in una fase a letto fluidizzato, la premiscelazione generalmente non è necessaria. Il materiale da granulare viene alimentato nel letto fluido, dove subisce una fase di preriscaldamento (temperatura adeguata alle caratteristiche del prodotto) per ottenere la prima miscelazione. Non è richiesto alcun test di uniformità dopo la fase di preriscaldamento, consentendo la granulazione diretta in una sola fase. Questo processo sfrutta il principio operativo del letto fluidizzato, in cui il materiale rimane in uno stato di ebollizione continuo, con una vigorosa miscelazione che avviene durante entrambe le fasi di preriscaldamento e granulazione.
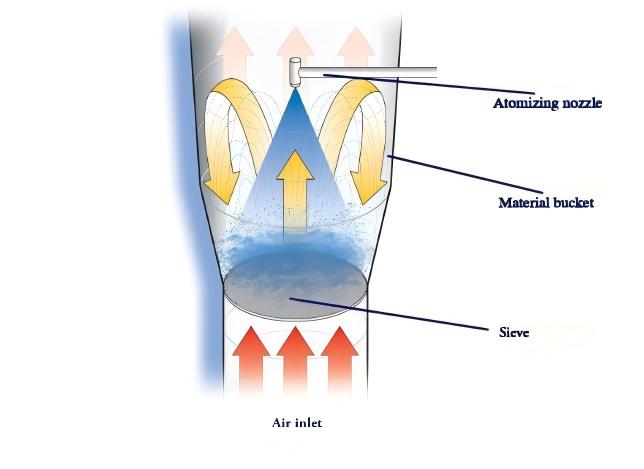
Durante la fase di preriscaldamento, l'assenza di aggiunta di legante può causare stratificazione tra materiali di diversa densità, rendendo impraticabile la valutazione dell'uniformità dopo il preriscaldamento. Nella successiva fase di granulazione, man mano che il legante viene atomizzato e introdotto, materiali di diversa densità vengono legati tra loro formando progressivamente particelle omogenee. Dopo la granulazione e l'essiccazione, sono necessarie operazioni come il soffiaggio del filtro a maniche per migliorare la resa del prodotto. Di conseguenza, polvere fine residua o piccole particelle rimangono inevitabilmente nello strato superiore del materiale dopo lo spegnimento della macchina. Pertanto, l'uniformità del contenuto ottenuta attraverso la granulazione a letto fluidizzato in una sola fase potrebbe non soddisfare i requisiti specificati nelle linee guida.
Le particelle prodotte attraverso la granulazione one-step a letto fluidizzato possono essere sottoposte a granulazione a secco o procedere direttamente al processo masterbatch, che garantisce un contenuto uniforme prima della compressione/riempimento delle compresse. Pertanto, nei processi di granulazione in una fase a letto fluidizzato, sia per test pilota, produzione su scala pilota o convalida del processo, il controllo e la convalida dell'uniformità del contenuto possono essere omessi, con maggiore enfasi posta sulla stabilità della resa. Se persistono dubbi sull’uniformità dei contenuti, è consigliabile raccogliere dati per un’analisi retrospettiva piuttosto che stabilire criteri di accettazione rigorosi.
III. Granulazione a secco
Nei processi di granulazione a secco, la premiscelazione è fondamentale per ottenere una dimensione delle particelle uniforme, e richiede una ricerca mirata. A differenza della granulazione in un unico passaggio a letto fluidizzato, la granulazione a secco dimostra un'efficienza di miscelazione più debole. Lo stadio del trasportatore a coclea raggiunge solo una miscelazione localizzata e la condizione di miscelazione dei materiali immessi nella tramoggia determina in ultima analisi l'uniformità dei granuli secchi.
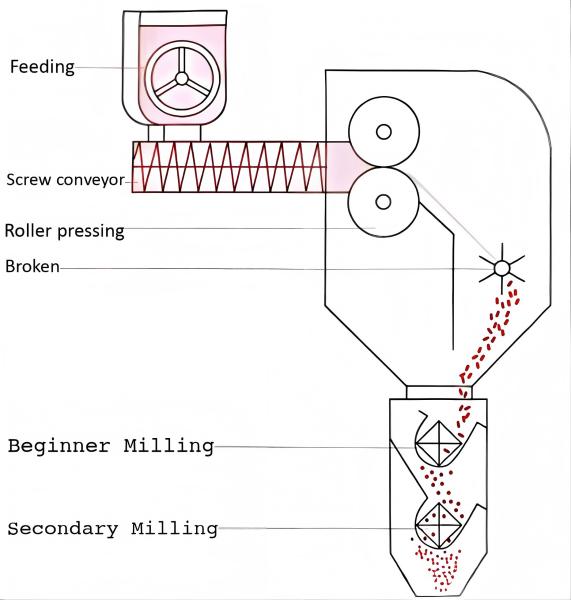
Nel caso della granulazione a secco dopo la miscelazione delle polveri, lo studio di pre-miscelazione e lo studio di miscelazione totale sono essenzialmente coerenti. Poiché lo stesso miscelatore può essere utilizzato sia per la premiscelazione che per la miscelazione totale, in genere non si verificano problemi relativi ai sottolotti durante la granulazione a secco dopo la miscelazione delle polveri. Le posizioni di campionamento dei mixer con principi diversi sono mostrate nella figura seguente.
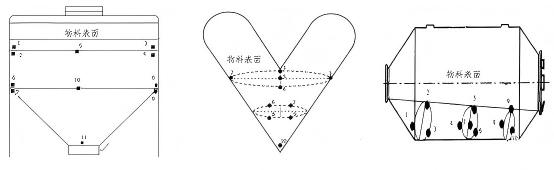
La granulazione a secco viene applicata principalmente alla granulazione a letto fluidizzato in un unico passaggio quando alcuni tipi di prodotti presentano una bassa densità (ad esempio, dispersioni solide preparate tramite letto fluidizzato), richiedendo un aumento della densità attraverso la granulazione a secco per un riempimento efficace o una compressione delle compresse. Potrebbe verificarsi un'elaborazione sub-batch in sistemi a letto fluidizzato. Poiché la granulazione a secco richiede in genere additivi esterni, è possibile combinare più sottolotti di materiali a letto fluidizzato con questi additivi prima della lavorazione. La valutazione dell'uniformità della premiscelazione per i materiali combinati segue la stessa metodologia della precedente procedura di miscelazione delle polveri.
Similmente al processo di granulazione a umido ad alto taglio, è possibile determinare la stessa quantità di caricamento della premiscela e la stessa velocità di miscelazione fissa in base al lotto di registrazione. Dai test pilota di laboratorio ai test pilota di officina, è possibile studiare solo l'impatto del tempo di miscelazione. Sulla base della ricerca pilota di laboratorio, il tempo di premiscelazione appropriato viene confermato durante il lotto pilota. Per i prodotti a basso rischio, durante la fase di validazione del processo viene condotta una sola verifica puntuale dell'uniformità della premiscelazione e la verifica dell'uniformità della premiscelazione può essere omessa.
IV. Pressatura/riempimento diretto di polveri
Il processo di compressione/riempimento diretto delle polveri richiede elevate proprietà del materiale per la qualità della formulazione. Tipicamente, ci sono due fasi di miscelazione: premiscelazione e miscelazione finale, con più fasi di miscelazione che precedono la fase finale. Nella maggior parte dei casi, durante la fase di miscelazione finale viene aggiunta solo una piccola quantità di lubrificante o di fluido ausiliario. Pertanto, è essenziale valutare l'uniformità della miscelazione attraverso indagini di premiscelazione e miscelazione prima della miscelazione finale. Vedere il diagramma schematico di campionamento nella sezione granulazione a secco.
L'indagine dell'omogeneità nel processo di premiscelazione/miscelazione mira principalmente a identificare parametri appropriati del tempo di miscelazione. Dato il numero limitato di processi diretti di pressatura/riempimento delle polveri, la produzione di convalida del processo può convalidare contemporaneamente sia la premiscelazione/miscelazione che la miscelazione finale per migliorare le capacità di controllo dei rischi per il processo di produzione.
Il processo di compressione/riempimento diretto della polvere può comportare più fasi di miscelazione e, ove possibile, la miscelazione manuale in una qualsiasi di queste fasi dovrebbe essere evitata. Per i prodotti ad alto rischio, la riproducibilità della produzione commerciale potrebbe non essere garantita a causa delle variazioni nelle competenze degli operatori.
V. Precauzioni per i processi misti
5.1 Criteri di accettazione
Per i farmaci convenzionali, l'uniformità totale della miscelazione deve generalmente essere entro ±10% (assoluto) del valore medio, con un coefficiente di variazione (RSD) ≤5%. Per i farmaci con indice terapeutico ristretto (NTI) o farmaci altamente attivi, dove l'accuratezza delle dosi unitarie ha un impatto significativo sull'efficacia e sulla sicurezza del farmaco, si raccomanda che i richiedenti la formulazione/produttori farmaceutici, sulla base della comprensione scientifica e della valutazione del rischio del prodotto, stabiliscano piani di campionamento più rigorosi, conducano studi sull'uniformità della miscelazione e sviluppino criteri di accettazione più rigorosi. Ad esempio, se l’RSD è fissato al 2% o anche a un livello inferiore e assumendo un coefficiente di variazione (CV) <10% per i farmaci NTI, un’uniformità del contenuto del 4,5% comporterebbe un rischio significativo di non equivalenza di bioequivalenza (BE). Fare riferimento alla sezione sull'analisi di equivalenza nella logica fondamentale del farmaco BE con finestra terapeutica ristretta. Indipendentemente dal processo di preparazione, ottenere lo stesso standard di uniformità di pre-miscelazione dell'uniformità di miscelazione totale è uno stato ideale. Se l'uniformità della premiscelazione non può soddisfare gli standard pertinenti, non c'è motivo di preoccuparsi, poiché l'intervallo accettabile per l'uniformità della premiscelazione può essere più ampio dei requisiti specificati nelle linee guida, a condizione che l'uniformità totale della miscelazione sia conforme ai requisiti delle linee guida.
5.2 tempo di miscelazione
In pratica, la miscelazione totale prevede tipicamente la sola aggiunta di stearato di magnesio come lubrificante, con una percentuale in peso pari a circa l'1%. Alcuni professionisti del settore hanno osservato che la durata totale della miscelazione è fissata a 1 o 2 minuti, poiché l'omogeneità della fase di miscelazione precedente è già stata verificata prima della miscelazione totale. Anche se lo stearato di magnesio viene distribuito in modo non uniforme durante la miscelazione totale, tali incoerenze non possono essere rilevate attraverso il test di omogeneità della miscelazione totale. La durata totale della miscelazione di 1 o 2 minuti può semplicemente servire come rassicurazione psicologica. Uno stearato di magnesio disomogeneo può portare a variazioni di dissoluzione da lotto a lotto e può anche causare problemi di adesione, rendendo potenzialmente necessario un aumento del dosaggio di stearato di magnesio.
Come dovrebbe essere progettato? Per formulazioni senza eccessivi problemi di lubrificazione (dove la durezza della compressa è inferiore a quella prevista o la dissoluzione è ridotta), si consiglia di incorporare tutti i materiali esterni, compreso lo stearato di magnesio, nel masterbatch per la miscelazione simultanea. Questo approccio non solo elimina una fase di elaborazione, ma evita anche la necessità di due valutazioni di uniformità separate. Per le formulazioni potenzialmente soggette a lubrificazione eccessiva, è comunque possibile utilizzare un metodo di miscelazione in una fase per ottenere il tempo di miscelazione più breve per l'uniformità. Lo stearato di magnesio può quindi essere aggiunto durante la miscelazione finale del masterbatch secondo questo momento ottimale. Se il tempo di miscelazione più breve non riesce a risolvere il problema della lubrificazione eccessiva (assumendo che la lubrificazione sia realmente eccessiva piuttosto che un errore di valutazione causato da altri fattori), si dovrebbero prendere in considerazione lubrificanti alternativi.
5.3 Numero di campioni
Secondo le linee guida, per il masterbatch, dovrebbero essere raccolti almeno tre campioni da ciascun punto di campionamento. Alcuni prodotti potrebbero richiedere test supplementari di uniformità del masterbatch come parte degli standard di qualità del prodotto intermedio, che richiedono il controllo dell'uniformità del contenuto durante la futura produzione commerciale. Per le premiscele, che in genere vengono condotte solo durante la fase di ricerca e sviluppo e sono di natura di ricerca, sono sufficienti da 1 a 2 campioni per punto (per backup).
Il volume di campionamento per un singolo campione dovrebbe generalmente variare da 1 a 10 volte la dose unitaria. L'intero campione deve essere utilizzato per il test di omogeneità per evitare il campionamento secondario. Quando il volume di campionamento supera 3 volte la dose unitaria, è necessario fornire una giustificazione o prova scientifica. Questo perché un volume di campione maggiore di 3 volte la dose unitaria può mascherare una miscelazione non uniforme dovuta a un'eccessiva quantità di campione.
VI. Conclusione
Le linee guida menzionano che la ricerca dovrebbe essere condotta su varietà valutate come a rischio medio-alto nei processi di miscelazione o compressione/riempimento in base al principio della valutazione del rischio, combinato con le caratteristiche del prodotto e del processo produttivo. Ad esempio, la Farmacopea cinese richiede lo studio dell'uniformità di miscelazione per le forme di dosaggio solide chimiche orali (quantità etichettata <25 mg o contenuto di principio attivo <25%) che richiedono test di uniformità del contenuto, poiché il loro rischio di miscelazione è relativamente elevato. Pertanto, per le varietà a basso rischio, alcuni studi sul processo di premiscelazione possono essere ridotti.
Che si tratti di processi di premiscelazione o di miscelazione finale, tutti devono essere sottoposti a valutazioni e test rigorosi secondo gli standard più severi. Non ci sono dubbi su questo: dopo tutto, i revisori del CDE non si lamenteranno dell'eccessiva ricerca. Tuttavia, i direttori della produzione si concentreranno sull’efficienza e sui costi, in particolare durante le ispezioni dei processi intermedi per la futura produzione commerciale. Se l’approvazione del controllo qualità è obbligatoria per i prodotti intermedi prima di procedere, non solo riduce l’efficienza produttiva ma si discosta anche dal principio della qualità fin dalla progettazione. Come sviluppatori di farmaci, dobbiamo considerare sia le fasi di ricerca e sviluppo che quelle di produzione commerciale. Sulla base delle caratteristiche del prodotto e delle valutazioni del rischio, dovremmo stabilire adeguate strategie di controllo della qualità, compresi controlli specifici per posizione e indicatori sostitutivi.


















