Como deve ser avaliada a uniformidade da mistura da pré-mistura?
Em 18 de fevereiro de 2022, o Centro de Avaliação de Medicamentos (CDE) emitiu as “Diretrizes Técnicas para Pesquisa sobre Homogeneidade de Formas Farmacêuticas Sólidas Orais e Homogeneidade da Unidade Central de Controle (Ensaio)”, doravante denominadas “Diretrizes”. As Diretrizes concentram-se no processo de mistura final, que também se baseia no conceito geral de qualidade desde a concepção. Isso ocorre porque a homogeneidade da mistura final antes das operações de compressão ou enchimento é a base para garantir a uniformidade do conteúdo do produto final, e também é a etapa ideal para amostragem e realização de estudos de homogeneidade. Em princípio, o estudo de homogeneidade desta etapa não deve ser ignorado e o teste de uniformidade de conteúdo do produto final não deve ser realizado diretamente. É claro que qualquer operação de mistura durante o processo de produção pode ser avaliada quanto à homogeneidade, mas os requisitos e padrões de homogeneidade em outros processos não são explicitamente especificados nestas Diretrizes. O autor compartilha alguns insights e discussões baseadas em experiências práticas encontradas no trabalho.
Os processos de produção comuns para formas farmacêuticas sólidas orais incluem granulação úmida de alto cisalhamento, granulação em leito fluidizado em uma etapa, granulação seca e compressão/enchimento direto de pó. Os procedimentos de mistura na produção de formas farmacêuticas sólidas orais normalmente envolvem pelo menos duas etapas de mistura: pré-mistura e mistura final, com alguns produtos potencialmente exigindo mais de duas etapas de mistura. Embora o processo de mistura final seja geralmente consistente em diferentes métodos de produção, os níveis de risco durante a fase de pré-mistura variam devido aos diferentes princípios de produção, necessitando de abordagens de investigação diferenciadas para a uniformidade da pré-mistura. De acordo com a edição de 2023 das Diretrizes GMP – Seção de Formas de Dosagem Sólidas Orais, não há nenhum requisito obrigatório para avaliar a uniformidade da mistura durante a pré-mistura (se aplicável). Determinar adequadamente a extensão da pesquisa de uniformidade de mistura é fundamental para os custos de desenvolvimento de produtos e controle de qualidade.
I. Granulação úmida de alto cisalhamento
Ao usar o processo de granulação úmida de alto cisalhamento, a etapa de pré-mistura deve ser idealmente realizada dentro do granulador úmido. Alternativamente, os materiais podem primeiro ser misturados num misturador antes de serem transferidos para o granulador. A menos que o produto tenha requisitos específicos, recomenda-se a pré-mistura no granulador, pois reduz a transferência de material e o uso do misturador, garantindo um fluxo de trabalho mais eficiente. Para granulação úmida de alto cisalhamento, a pré-mistura normalmente é essencial, pois minimiza o risco de grânulos úmidos irregulares nas etapas subsequentes do processamento.
Princípios de amostragem baseados em princípios orientadores: Os pontos de amostragem devem ser uniformemente distribuídos e representativos. Considerando as características estruturais do equipamento de mistura, as zonas mortas do equipamento de mistura devem ser identificadas para garantir a cobertura de todos os materiais, representando ao mesmo tempo os locais de pior caso. Os pontos de amostragem de pré-mistura dentro do granulador úmido são mostrados na figura abaixo.
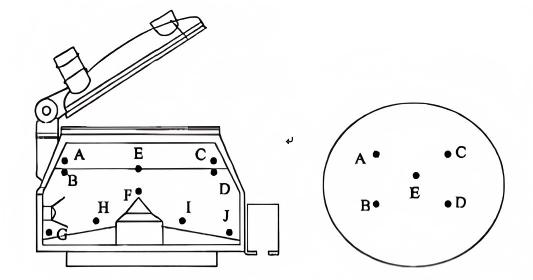
A homogeneidade da pré-mistura é geralmente influenciada por quatro fatores: volume de carga do material, velocidade de agitação, taxa de cisalhamento e tempo de mistura, com potenciais interações entre eles. A realização de um Projeto de Experimentos (DOE) exigiria um número excessivo de tentativas. O volume de carregamento pode ser calculado com base no tamanho final do lote de registro para garantir a consistência entre lotes de laboratório e lotes de registro futuros. A velocidade de agitação e a taxa de cisalhamento podem ser determinadas considerando o estado de mistura dos materiais e a relação entre o raio da pá de agitação entre equipamentos de escala piloto e de escala intermediária. Essa abordagem reduz variáveis multifatoriais a um único parâmetro – tempo de mistura – para análise.
A fase inicial envolve estudos laboratoriais para avaliar como diferentes durações de pré-mistura afetam a uniformidade do produto, permitindo a identificação de parâmetros ideais. Esses parâmetros são então validados durante a produção em escala piloto. Nas operações piloto, as amostras são coletadas em vários intervalos de pré-mistura para avaliar a consistência, garantindo a compatibilidade entre os tempos de mistura em laboratório e em escala piloto. Para validação do processo, apenas um ponto no tempo é necessário, já que os parâmetros de pré-mistura são normalmente definidos como valores fixos em vez de intervalos. Notavelmente, a validação da uniformidade da pré-mistura é muitas vezes omitida nesta fase (particularmente para produtos de baixo risco com quantidades rotuladas> 25 mg ou conteúdo de ingrediente ativo> 25%), uma vez que a duração da mistura é predeterminada na produção piloto e subsequentes testes de uniformidade total da mistura serão realizados.
Com base em nossa experiência em P&D em equipamentos de laboratório, estabelecemos diretrizes preliminares para um tempo de mistura ideal. Durante a amostragem de uniformidade de pré-mistura do lote piloto, não precisamos mais coletar três amostras por ponto, conforme protocolos padrão. Este ajuste ocorre porque a avaliação do lote piloto se concentra em avaliar como diferentes durações de mistura afetam a uniformidade. Mesmo quando o RSD (desvio padrão relativo) em pontos de tempo mais baixos parece significativo, não há necessidade de validar as duas amostras restantes com base nos resultados da medição. Em vez disso, devemos selecionar o ponto de tempo ideal que demonstre a maior uniformidade.
Para produtos de granulação de sublotes, se a uniformidade de pré-mistura dos sublotes tiver sido estudada em lotes piloto com boa reprodutibilidade entre sublotes, isso indica processos de pré-mistura estáveis. Mesmo para produtos com teor de ingrediente farmacêutico ativo (IFA) inferior a 25%, os riscos de pré-mistura são considerados baixos, e a validação da uniformidade da pré-mistura pode ser omitida nos lotes de validação do processo. O pessoal da linha de frente deve estar ciente de que a fase de validação envolve volumes de amostras excepcionalmente grandes e quantidades de testes em prazos apertados. Através da avaliação de riscos, podemos alocar recursos para processos de alto risco para controlar melhor a qualidade do produto.
II. Granulação em uma etapa em leito fluidizado
Na granulação de um passo em leito fluidizado, a pré-mistura é geralmente desnecessária. O material a ser granulado é alimentado no leito fluidizado, onde passa por uma fase de pré-aquecimento (temperatura ajustada de acordo com as características do produto) para obter a mistura inicial. Nenhum teste de uniformidade é necessário após o estágio de pré-aquecimento, permitindo granulação direta em uma única etapa. Este processo aproveita o princípio operacional do leito fluidizado, onde o material permanece em estado de ebulição contínua, ocorrendo uma mistura vigorosa durante as fases de pré-aquecimento e granulação.
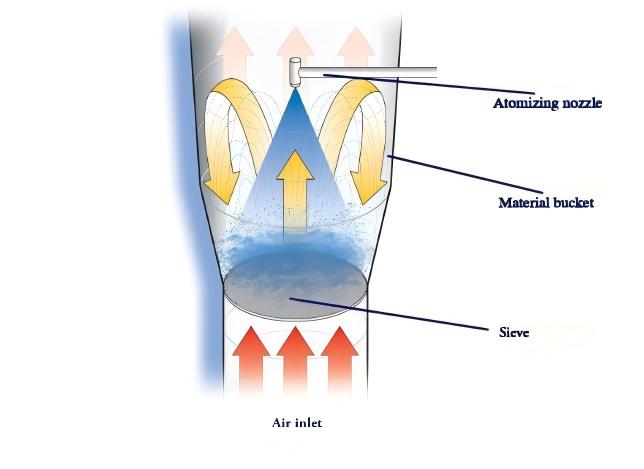
Durante a etapa de pré-aquecimento, a ausência de adição de ligante pode causar estratificação entre materiais de diferentes densidades, tornando impraticável a avaliação da uniformidade após o pré-aquecimento. Na fase de granulação subsequente, à medida que o ligante é atomizado e introduzido, materiais de densidades variadas são unidos, formando gradualmente partículas homogêneas. Após a granulação e a secagem, operações como o contra-sopro do filtro de mangas são necessárias para melhorar o rendimento do produto. Consequentemente, pó fino residual ou pequenas partículas permanecem inevitavelmente na camada superior do material após o desligamento da máquina. Portanto, a uniformidade de conteúdo obtida através da granulação em leito fluidizado em uma única etapa pode não atender aos requisitos especificados nas diretrizes.
As partículas produzidas através da granulação em uma etapa em leito fluidizado podem sofrer granulação a seco ou prosseguir diretamente para o processo masterbatch, o que garante conteúdo uniforme antes da compressão/envase do comprimido. Portanto, em processos de granulação de uma etapa em leito fluidizado – seja para testes piloto, produção em escala piloto ou validação de processo – o controle e validação da uniformidade de conteúdo podem ser omitidos, com maior ênfase na estabilidade do rendimento. Se persistirem preocupações com a uniformidade do conteúdo, é aconselhável recolher dados para análise retrospetiva em vez de estabelecer critérios de aceitação rigorosos.
III. Granulação Seca
Nos processos de granulação a seco, a pré-mistura é fundamental para atingir um tamanho de partícula uniforme, exigindo pesquisa focada. Ao contrário da granulação de uma etapa em leito fluidizado, a granulação seca demonstra uma eficiência de mistura mais fraca. O estágio do transportador helicoidal atinge apenas a mistura localizada, e a condição de mistura dos materiais alimentados na tremonha determina, em última análise, a uniformidade dos grânulos secos.
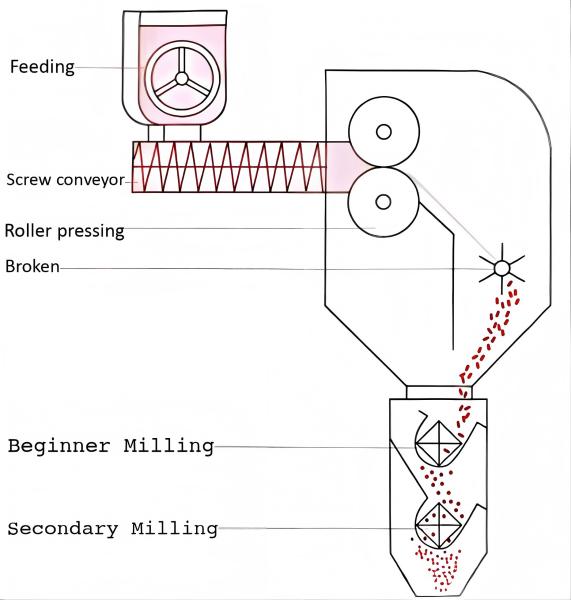
Para o caso de granulação seca após mistura do pó, o estudo de pré-mistura e o estudo de mistura total são essencialmente consistentes. Como o mesmo misturador pode ser usado tanto para pré-mistura quanto para mistura total, problemas de sublote geralmente não ocorrem durante a granulação a seco após a mistura do pó. As posições de amostragem de misturadores com diferentes princípios são mostradas na figura abaixo.
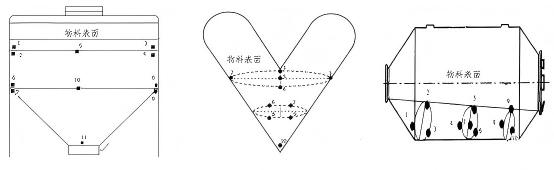
A granulação seca é aplicada principalmente à granulação em leito fluidizado de etapa única quando certos tipos de produtos apresentam baixa densidade (por exemplo, dispersões sólidas preparadas via leito fluidizado), exigindo aumento de densidade através de granulação seca para enchimento ou compressão de comprimidos bem-sucedidos. Pode ocorrer processamento em sublote em sistemas de leito fluidizado. Uma vez que a granulação seca normalmente requer aditivos externos, múltiplos sublotes de materiais de leito fluidizado podem ser combinados com estes aditivos antes do processamento. A avaliação da uniformidade da pré-mistura para os materiais combinados segue a mesma metodologia do procedimento anterior de mistura do pó.
Semelhante ao processo de granulação úmida de alto cisalhamento, a mesma quantidade de carregamento de pré-mistura e velocidade de mistura fixa podem ser determinadas com base no lote de registro. Desde testes piloto de laboratório até testes piloto de oficina, apenas o impacto do tempo de mistura pode ser estudado. Com base na pesquisa piloto de laboratório, o tempo de pré-mistura apropriado é confirmado durante o lote piloto. Para produtos de baixo risco, apenas uma verificação pontual da uniformidade da pré-mistura é realizada durante a fase de validação do processo, e a verificação da uniformidade da pré-mistura pode ser omitida.
4. Prensagem/Enchimento Direto de Pós
O processo de compressão/envase direto do pó requer altas propriedades do material para a qualidade da formulação. Normalmente, existem dois estágios de mistura: pré-mistura e mistura final, com múltiplas etapas de mistura precedendo o estágio final. Na maioria dos casos, apenas uma pequena quantidade de lubrificante ou auxiliar de fluxo é adicionada durante a etapa final de mistura. Portanto, é essencial avaliar a uniformidade da mistura através de investigações de pré-mistura e mistura antes da mistura final. Veja o diagrama esquemático de amostragem na seção de granulação seca.
A investigação da homogeneidade no processo de pré-mistura/mistura visa principalmente identificar parâmetros de tempo de mistura apropriados. Dado o número limitado de processos diretos de prensagem/enchimento de pó, a produção de validação do processo pode validar simultaneamente tanto a pré-mistura/mistura quanto a mistura final para aprimorar as capacidades de controle de risco para o processo de fabricação.
O processo de compressão/enchimento direto do pó pode envolver múltiplas etapas de mistura, e a mistura manual em qualquer uma dessas etapas deve ser evitada sempre que possível. Para produtos de alto risco, a reprodutibilidade da produção comercial pode não ser garantida devido a variações nas competências dos operadores.
V. Precauções para Processos Mistos
5.1 Critérios de Aceitação
Para medicamentos convencionais, geralmente é necessário que a uniformidade total da mistura esteja dentro de ±10% (absoluto) do valor médio, com um coeficiente de variação (RSD) ≤5%. Para medicamentos de índice terapêutico estreito (NTI) ou medicamentos altamente ativos, onde a precisão das doses unitárias impacta significativamente a eficácia e segurança do medicamento, recomenda-se que os requerentes de formulação/fabricantes farmacêuticos, com base na compreensão científica e na avaliação de risco do produto, estabeleçam planos de amostragem mais rigorosos, conduzam estudos de uniformidade de mistura e desenvolvam critérios de aceitação mais rigorosos. Por exemplo, se o RSD for fixado em 2% ou até menos, e assumindo um coeficiente de variação (CV) <10% para medicamentos NTI, uma uniformidade de conteúdo de 4,5% representaria um risco significativo de não equivalência de bioequivalência (BE). Consulte a seção de análise de equivalência na lógica fundamental do medicamento BE com janela terapêutica estreita. Independentemente do processo de preparação, alcançar o mesmo padrão de uniformidade de pré-mistura e uniformidade total de mistura é um estado ideal. Se a uniformidade da pré-mistura não puder atender aos padrões relevantes, não há necessidade de preocupação, pois a faixa aceitável para a uniformidade da pré-mistura pode ser mais ampla do que os requisitos especificados nas diretrizes, desde que a uniformidade total da mistura esteja em conformidade com os requisitos das diretrizes.
5.2 tempo de mistura
Na prática, a mistura total envolve tipicamente apenas a adição de estearato de magnésio como lubrificante, com uma percentagem em peso de aproximadamente 1%. Alguns profissionais da indústria observaram que a duração total da mistura é fixada em 1 ou 2 minutos, uma vez que a homogeneidade da fase de mistura anterior já foi verificada antes da mistura total. Mesmo que o estearato de magnésio seja distribuído de forma desigual durante a mistura total, tais inconsistências não podem ser detectadas através do teste de homogeneidade da mistura total. A duração total da mixagem de 1 ou 2 minutos pode servir simplesmente como uma garantia psicológica. O estearato de magnésio não homogêneo pode levar a variações de dissolução entre lotes e também pode resultar em problemas de adesão, necessitando potencialmente de aumento da dosagem de estearato de magnésio.
Como isso deve ser projetado? Para formulações sem problemas excessivos de lubrificação (onde a dureza do comprimido está abaixo do esperado ou a dissolução é reduzida), recomenda-se incorporar todos os materiais externos, incluindo estearato de magnésio, no masterbatch para mistura simultânea. Esta abordagem não apenas elimina uma etapa de processamento, mas também evita a necessidade de duas avaliações de uniformidade separadas. Para formulações potencialmente propensas a lubrificação excessiva, um método de mistura em uma etapa ainda pode ser empregado para obter o menor tempo de mistura para uniformidade. O estearato de magnésio pode então ser adicionado durante a mistura final do masterbatch de acordo com este tempo ideal. Se o menor tempo de mistura não resolver o problema de lubrificação excessiva (assumindo que a lubrificação é genuinamente excessiva e não um erro de julgamento causado por outros fatores), lubrificantes alternativos devem ser considerados.
5.3 Número de Amostras
De acordo com as diretrizes, para masterbatch, pelo menos três amostras devem ser coletadas em cada ponto de amostragem. Alguns produtos podem exigir testes suplementares de uniformidade de masterbatch como parte dos padrões intermediários de qualidade do produto, o que exige controle de uniformidade de conteúdo durante a produção comercial futura. Para pré-misturas, que normalmente são realizadas apenas durante a fase de pesquisa e desenvolvimento e são de natureza de pesquisa, 1 a 2 amostras por ponto (para backup) são suficientes.
O volume de amostragem para uma única amostra deve normalmente variar de 1 a 10 vezes a dose unitária. Toda a amostra deve ser usada para testes de homogeneidade para evitar amostragem secundária. Quando o volume de amostragem exceder 3 vezes a dose unitária, deverá ser fornecida uma justificativa ou evidência científica. Isso ocorre porque um volume de amostra maior que 3 vezes a dose unitária pode mascarar o fato de mistura desigual devido à quantidade excessiva de amostra.
VI. Conclusão
As diretrizes mencionam que a pesquisa deve ser realizada em variedades avaliadas como de médio a alto risco em processos de mistura ou compressão/envase com base no princípio da avaliação de risco, combinado com as características do produto e do processo de produção. Por exemplo, a Farmacopeia Chinesa exige o estudo da uniformidade de mistura para formas farmacêuticas sólidas orais químicas (quantidade rotulada <25 mg ou conteúdo de ingrediente ativo <25%) que exigem testes de uniformidade de conteúdo, pois o risco de mistura é relativamente alto. Portanto, para variedades de baixo risco, alguns estudos do processo de pré-mistura podem ser reduzidos.
Quer se trate de processos de pré-mistura ou de mistura final, todos devem passar por avaliações e testes rigorosos sob os mais rígidos padrões. Não há dúvida sobre isso – afinal, os revisores do CDE não reclamarão do excesso de pesquisa. No entanto, os diretores de produção concentrar-se-ão na eficiência e nos custos, especialmente durante as inspeções de processos intermédios para a produção comercial futura. Se a aprovação do CQ for obrigatória para produtos intermediários antes de prosseguir, isso não apenas reduzirá a eficiência da produção, mas também se desviará do princípio da qualidade desde o projeto. Como desenvolvedores de medicamentos, devemos considerar as fases de pesquisa e desenvolvimento e de produção comercial. Com base nas características do produto e nas avaliações de risco, devemos estabelecer estratégias adequadas de controlo de qualidade, incluindo controlos específicos da posição e indicadores substitutos.


















